:醇和氯化亚砜的反应(2015年03月23日)
醇与亚硫酰氯的反应过程首先形成氯亚硫酸盐(4),然后断裂CO键释放出二氧化硫,生成氯化烃。 (4)的分解方式与溶剂的极性有关,同时决定了氯化反应过程中醇碳原子构型的变化。 例如,在二恶烷中反应时,二恶烷氧原子上的未共享电子对从酯基的反位与酯碳原子形成弱键,增加了反位方向的空间位阻,促进了反应的进行。氯离子的作用。 SNi取代导致保留醇碳原子的原始构型; 然而,如果反应在吡啶中进行,则氯化氢和吡啶形成盐并储存在反应溶液中。 酯基反应中解离的氯离子可用作SN2。 代入,得到配置翻转的产品; 如果没有溶剂,(4)在某些催化剂(如氯化锌)的作用下直接分解成离子对形式,根据SN1机理得到外消旋产物。
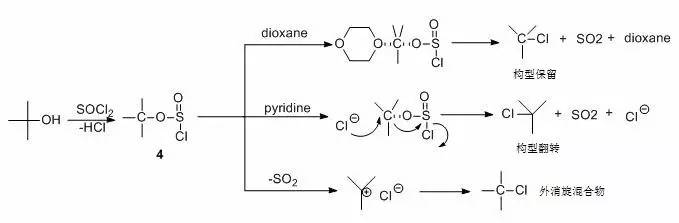
例如,旋光2-正辛醇与亚硫酰氯在不同溶剂中反应,得到相应不同构型的氯化物。 如果加入氯化锌作为催化剂,反应速率显着加快,SNi机理转变为SN1机理。 ,得到外消旋产物。
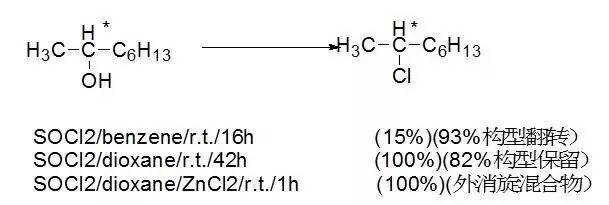

烯丙醇与亚硫酰氯在乙醚中反应时,烯丙基重排产物的比例与所用亚硫酰氯的浓度有关。 例如,化合物2-丁烯-1-醇(5)在5.6摩尔氯化亚砜醚溶液中得到两种双键位置不同的异构体混合物; 而当使用0.7mol氯化亚砜时,几乎完全是重排产物,这可能是由于无水乙醚在稀溶液中容易与干燥氯化氢形成氢键配合物,有利于SN1反应和双键重排。
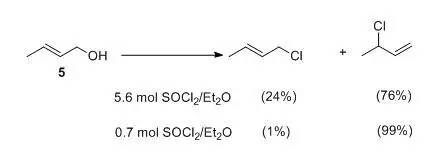
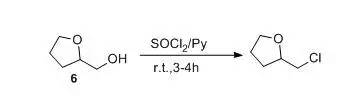
在亚硫酰氯的反应中苯甲醇与醇反应,如果加入有机碱(如吡啶)作为催化剂,或者醇本身存在氨基等碱性基团,可以与反应中生成的氯化氢结合,因此有利于氯化反应的改善。 速度。 此外,该反应还适用于一些对酸敏感的醇的氯置换反应。 例如,2-羟甲基四氢呋喃(6)与氯化亚砜和吡啶在室温下反应,得到预期的2-氯甲基四氢呋喃,且不影响酯环醚结构。
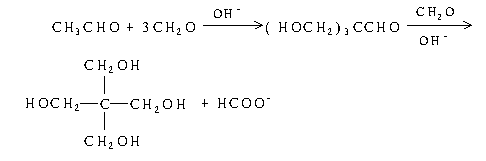
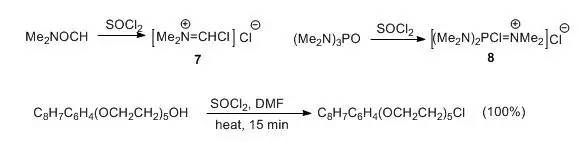
当SOCl2与DMF或HMPA(催化剂和溶剂)一起使用时,氯化剂的实际形式为(7)或(8)。 由于它们具有活性高、反应速度快、选择性好、能够有效结合反应中生成的HCl等优点,特别适用于某些有特殊要求的醇式羟基氯化物置换反应,也可作为良好的替代品。羧基羟基氯化物置换试剂。 。
反应示例
答:10-(4-)
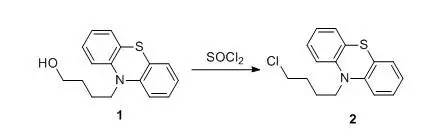
添加1(2.03g,7.5mmol)的100ml干燥溶液(2ml,)。 是在房间里。 到下。 将其置于凝胶上并用10%乙基进行洗脱,得到2.17g(62%)的2。
, 2002, 45,13, 2741-2748
乙:1-
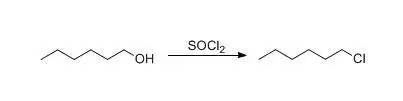
在一个500毫升的三烧瓶中,带有一个单元,和一个; 安装保护管。 将 179 g(109.5 ml,1.5 mol)的 1-己醇放入烧瓶中,将 51 g(62.5 ml,0.5 mol)的 1-己醇放入 1-己醇中。 添加2小时; 的热量苯甲醇与醇反应,以及 . 当所有的都完成后,需要2个小时。
的,和; 80℃,由a升至120℃;粗品1-在132-134℃。 用 10% 的水清洗 las-named。 用 和 干燥。 133-134℃纯1-以上。 产量为36克(60%)。
, 第 4 名,558
本站对作者上传的所有内容将尽可能审核来源及出处,但对内容不作任何保证或承诺。请读者仅作参考并自行核实其真实性及合法性。如您发现图文视频内容来源标注有误或侵犯了您的权益请告知,本站将及时予以修改或删除。



