第一批鼓励仿制药建议清单发布 2019年我国仿制药迎政策红利(附政策)
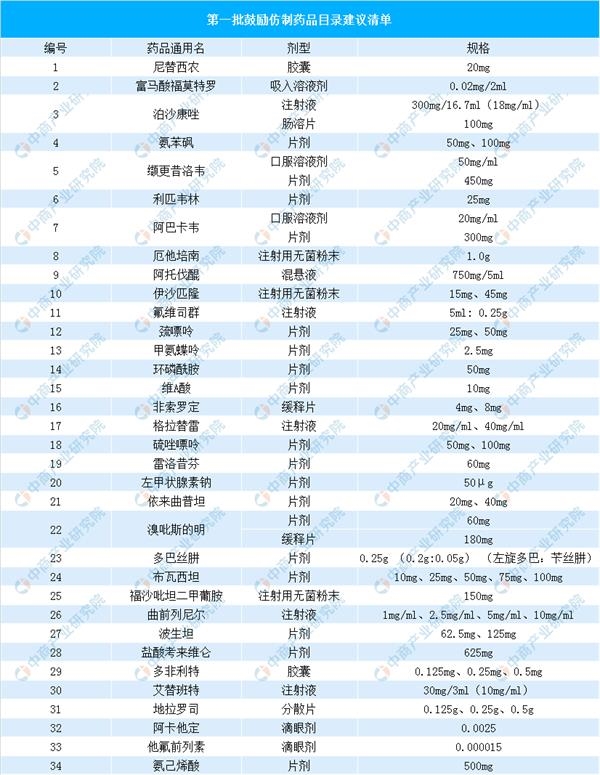
日前,国家卫健委于公示了《第一批鼓励仿制药品目录建议清单》,清单内共34种药物,包括艾滋病治疗药物利匹韦林、阿巴卡韦和白血病治疗药物硫唑嘌呤。制定目录有利于解决原研药价格过高、药品短缺问题。
仿制药是指专利药品在专利保护期结束后,不拥有该专利的药企仿制的替代药品。仿制药与原研药具有相同的活性成分、剂型、给药途径和治疗作用。很多原研药价格昂贵,重症患者无力负担,价格便宜很多的仿制药成了他们的救命稻草。贫困患者迫切需要仿制药,但仿制药的供应和使用却遇到各种各样的障碍。仿制药在中国药品市场中扮演着日益重要的角色。中国医药工业信息中心测算得出,2016年中国仿制药市场规模约为9167亿元,受人口老龄化和医保控费等因素的影响,中国仿制药市场规模将持续增长。至2020年,其市场规模可能达到14116亿元。
国家也正鼓励高品质仿制药的发展。早在2012年1月份,国务院就曾印发《国家药品安全“十二五”规划的通知》,提出其主要任务与目标之一是全面提高仿制药质量,“分期分批与被仿制药进行质量一致性评价,其中纳入国家基本药物目录、临床常用的仿制药在2015年前完成,未通过质量一致性评价的不予再注册,注销其药品批准证明文件。”2016年3月5日,国务院下发《关于开展仿制药质量与疗效一致性评价的意见》,单独出台针对性政策,标志我国仿制药一致性评价的改革大幕正式拉开。2017年一致性评价相关政策也跟着进一步落地与完善。
进入到2018年,中国医药行业步入新的发展阶段,仿制药通过国家一致性评价实现进口替代。
2018年4月,国务院《关于改革完善仿制药供应保障及使用政策的意见》的发布,无疑将对我国仿制药产业带来了指导性意见。《意见》明确了鼓励仿制药的药品范围:“临床必需、疗效确切、供应短缺”的药品。此外,鼓励仿制重大传染病防治和罕见病治疗所需药品、处置突发公共卫生事件所需药品、儿童使用药品以及专利到期前一年尚没有提出注册申请的药品。
另外,12月国家卫生健康委等12部门发布的《关于印发加快落实仿制药供应保障及使用政策工作方案的通知》,其中提出,要及时发布鼓励仿制的药品目录。根据临床用药需求,2019年6月底前,发布第一批鼓励仿制的药品目录,引导企业研发、注册和生产。2020年起,每年年底前发布鼓励仿制的药品目录。



